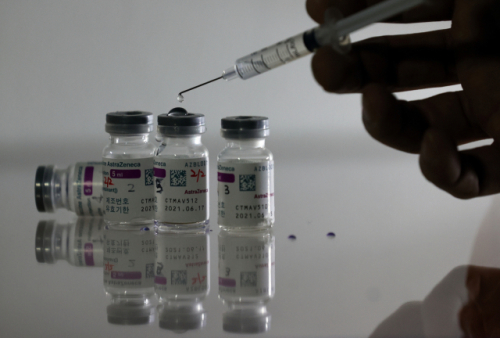
식품의약품안전처가 아스트라제네카(AZ)의 신종 코로나바이러스 감염증(코로나19) 백신에 대해 마지막 품질 검정 단계인 국가출하승인 절차를 17일 완료했다.
백신은 품목허가와 별개로 유통 또는 시판되기 전에 품질을 확인하는 국가출하승인 절차를 통과해야 한다. 아스트라제네카의 코로나19 백신은 지난 10일 식약처의 품목허가를 받았고 이후 국가출하승인 절차를 밟아왔다. 이날 국가출하승인 절차를 최종적으로 통과해 26일부터 접종이 시작된다.
식약처는 이 백신에 대해 만 18세 이상 성인에 모두 쓸 수 있다고 허가했다. 단 만 65세 이상 고령자에 대한 투여는 신중하게 결정해야 한다는 조건을 붙였다. 안전성에는 문제가 없으나 고령자에 대한 예방효과를 판단할 만한 임상시험 결과가 부족해 충분한 근거가 없다고 판단했기 때문이다.
정부는 이 백신을 당분간 만 65세 미만에 우선 접종한다는 계획을 세웠다. 만 65세 이상 고령자 접종 계획은 이 백신의 예방효과와 관해 추후 발표될 임상정보 등을 확인한 후 예방접종전문위원회 심의를 거쳐 확정할 예정이다.
이에 따라 오는 26일부터 전국의 요양병원과 요양시설 등에서 만 65세 미만의 입소자 및 종사자를 대상으로 아스트라제네카 코로나19 백신 접종이 시작될 예정이다. 접종되는 물량은 국내 백신 기업인 SK바이오사이언스에서 위탁 생산한다.
한편 식약처는 화이자의 코로나19 백신 품목허가 심사에도 속도를 내고 있다. 화이자는 지난달 25일 식약처에 코로나19 백신의 품목허가를 신청했다. 최근 특례수입을 승인받은 코백스 퍼실리티(COVAX facility)의 화이자 백신과는 별개다.
식약처는 이달 넷째 주 이후로 화이자의 코로나19 백신에 대한 '3중'의 전문가 자문절차를 진행할 계획이다. 예정대로라면 3월 첫째 주 이후에 허가를 받게 된다.
/박신원 인턴기자 shin01@sedaily.com
< 저작권자 ⓒ 서울경제, 무단 전재 및 재배포 금지 >