삼성바이오에피스와 셀트리온(068270)이 바이오시밀러 ‘세컨웨이브’ 라인업 구축을 마치고 본격적인 시장 주도권 경쟁에 나선다. 현재 임상 3상이 진행중인 제품 모두 오리지널 의약품 특허가 2028년 이후 만료돼 3년간 신규 제품 없이 보릿고개를 넘어야 하는 형국이다. 인허가를 마친 기존 제품에 대한 마케팅 역량이 미국 시장에서 승부를 가를 것으로 예상된다.
22일 제약·바이오업계에 따르면 삼성에피스는 그동안 준비해 온 11개 바이오시밀러들 중 10개 제품에 대해 미국 식품의약국(FDA) 인허가를 마쳤고 셀트리온은 12개 제품 중 11개 제품에 대해 FDA 인허가를 완료했다. 키트루다 바이오시밀러 전까지 남은 파이프라인은 삼성에피스의 경우 SB8로 인허가를 잠정 중단한 것으로 알려졌다. 셀트리온은 아일리아 바이오시밀러의 인허가를 진행하고 있으나 오리지널사인 리제네론과 소송이 변수로 떠오른 상황이다.
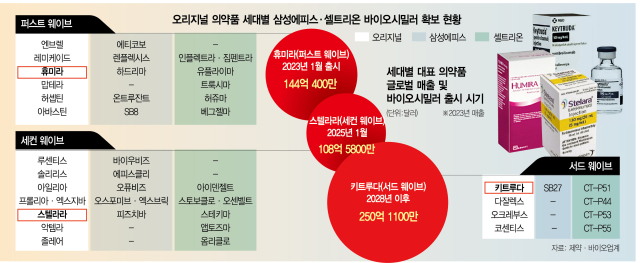
양사 모두 당분간 신규 허가 제품이 없는 만큼 업계에서는 마케팅 전략이 승부를 가를 것으로 보고있다. 바이오업계 관계자는 “2028년 전까지 새롭게 출시될 바이오시밀러 제품이 거의 없어 일종의 보릿고개를 넘어야 하는 상황”이라며 "기존 제품의 판매량을 늘리는 게 무엇보다 중요해졌다”고 말했다. 현재 임상 3상이 진행 중인 제품은 삼성에피스의 경우 키트루다(2028년), 셀트리온의 경우 키트루다, 다잘렉스(2028년), 오크레부스(2029년), 코센티스(2029년) 바이오시밀러로 모두 2028년 이후 미국에서 특허가 만료된다.
글로벌 업계와 정면 승부를 위한 라인업은 모두 갖춘 상태다. 삼성에피스는 현재까지 미국에서 총 6개 제품을 미국에 출시했다. 나머지 4개 제품은 오리지널사와 소송이 진행 중이어서 결과에 따라 출시 일정을 조정할 계획이다. 셀트리온은 현재까지 총 7개 제품을 시중에 선보였다. 올 6월에는 오리지널사 암젠과 최근 합의에 도달한 바이오시밀러 ‘스토보클로’와 ‘오센벨트’를 추가할 예정이다. ‘스테키마’와 ‘앱토즈마’ 출시 시기는 아직 공개되지 않았다.
최대 격전지는 존슨앤존슨의 ‘스텔라라’ 바이오시밀러 시장이다. 스텔라라는 미국에서만 20조 원 넘는 시장을 형성하고 있다. 삼성에피스와 셀트리온은 현지 3대 처방약급여관리업체(PBM) 중 일부와 협상을 마쳤다. 미국 3대 PBM은 ESI, CVS 케어마크, 옵텀으로 전체 PBM 시장의 약 80%를 점유하고 있다. PBM에 의약품이 등재돼야 보험 혜택을 받을 수 있기 때문에 미국 시장 진출을 위한 필수 통과 과정이다.
삼성에피스는 스위스 산도스와 파트너십을 맺고 미국 스텔라라 시밀러 시장을 공략한다. 산도스는 미국 PBM사 중 최대 점유율(21.3%)을 확보한 CVS 케어마크와 협력하고 있는 것으로 알려졌다. 삼성에피스 관계자는 “산도스는 앞서 유럽에서 ‘피즈치바’로 유럽 스텔라라 시밀러 시장 1위를 차지한 저력이 있다”며 “오리지널 대비 최대 80% 저렴한 가격으로 시장 공략에 나설 것”이라고 강조했다.
셀트리온은 미국 현지 법인을 통해 직접 판매 체계를 구축한 만큼 이를 적극 활용할 계획이다. PBM 등재 이후 현지 의사들을 상대로 직접 영업 활동을 진행할 수 있는 강점을 최대한 살린다는 전략이다. 셀트리온 관계자는 “해외 유통사를 거치면 수수료가 들어 그만큼 이익률은 감소한다”며 “'베그젤마'부터 미국에서 판매하는 모든 제품을 자체 유통망을 통해 판매하고 있기 때문에 시장 상황에 따라 마진을 조정해 다양한 마케팅 활동을 펼칠 수 있다"고 말했다.
< 저작권자 ⓒ 서울경제, 무단 전재 및 재배포 금지 >











 1min9@sedaily.com
1min9@sedaily.com






































