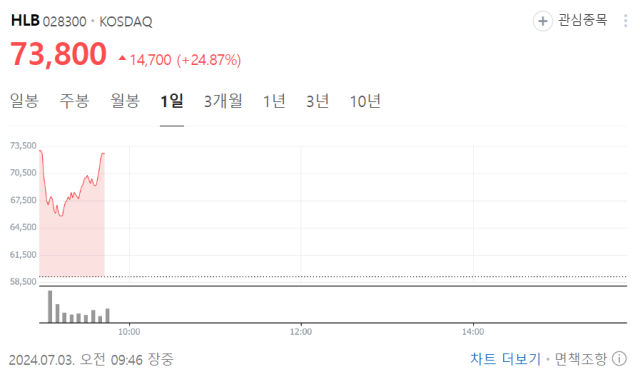
HLB(028300)는 간암 신약 리보세라닙의 허가심사 재개를 위한 미국식품의약국(FDA)과 미팅이 2일(미국시간) 완료됐다는 소식에 24%에 급등했다. 글로벌 허가에 대한 기대감이 다시 높아졌기 때문으로 분석된다.
이날 미팅은 HLB의 미국 자회사 엘레바와 항서제약이 참여했다. 회사 측에 따르면 FDA는 CRL(보완요청서신) 발급으로 지연됐던 본심사를 다시 속행하기 위해 “재심사 신청서를 제출할 것을 강력히 권고한다”는 입장과 함께 공식 문서(PAL·Post Action Letter)를 전달했다.
HLB 관계자는 “지난해 12월 간암신약 병용약물인 캄렐리주맙에 대한 화학·제조·품질관리(CMC) 현장실사 후 제기됐던 지적사항에 대해 이미 항서제약이 충실히 보완자료를 제출했다”며 “FDA가 추가적으로 요청하는 보완서류는 없다는 점을 뜻한다”고 설명했다.
항서는 별도 실험이나 서류의 준비 없이 실사 이후 두 차례에 걸쳐 제출한 보완 자료를 반영해 FDA에 BLA 서류를 제출하면 된다. FDA는 해당 서류를 접수 후 판단 기준에 따라 최대 2개월(Class 1) 또는 6개월(Class 2)로 심사기간을 정해 해당 기간 내 허가 여부를 결정하게 된다.
HLB는 이번 과정을 기회로 활용할 계획이다. 올해 미국종양학회(ASCO)에서 발표했던 글로벌 3상(CARES-310) 최종 임상 결과 데이터를 이번 재심사 요청 서류와 함께 제출할 계획이다. 최종 임상 결과, 환자의 전체생존기간(mOS)이 기존 22.1개월에서 23.8개월로 연장돼, 대조군이나 기존 치료제들과 비교 시 우월한 효능을 입증했다. 항서의 기존 보완서류와 함께 해당 서류도 제출목록에 포함시킨다는 구상이다.
간암신약에 대해 제기됐던 불확실성이 제거된 만큼, 회사는 이제 글로벌 허가를 위한 잔여 절차에 집중한다는 계획이다.
한용해 HLB그룹 최고기술경영자(CTO)는 “이번 미팅을 통해 FDA의 지적사항에 대해 이미 충분한 보완서류를 제출했다는 항서제약의 자신감이 사실로 확인된 만큼 회사는 빠른 시일내 재심사 요청서류를 완벽히 준비해 제출할 방침이다”며 “계획 대비 다소 지연이 발생했으나, 이번 기회로 생산공장에 대한 완벽한 점검을 진행해 제품의 품질에 대한 대외 신뢰성을 높일 수 있었고, 간암신약의 더 뛰어난 데이터도 공식적으로 반영할 수 있게 돼, 향후 긍정적인 효과가 있을 것으로 기대한다”고 말했다.
◇Why 바이오 코너는 증시에서 주목받는 바이오 기업들의 이슈를 전달하는 연재물입니다. 주가나 거래량 등에서 특징을 보인 제약·바이오 기업에 대해 시장이 주목한 이유를 살펴보고, 해당 이슈에 대해 해설하고 전망합니다.
< 저작권자 ⓒ 서울경제, 무단 전재 및 재배포 금지 >











 haena07@sedaily.com
haena07@sedaily.com





































