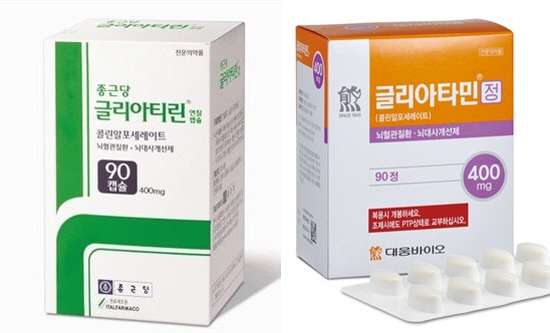
국내 대표적인 치매치료제인 ‘콜린알포세레이트(콜린알포)’의 임상 재평가 기한이 결국 연장됐다. 의정 갈등 장기화 속에 제약사들이 환자 모집에 어려움을 겪은 영향이다.
25일 제약·바이오업계에 따르면 식품의약품안전처는 이달 12일 중앙약사심의위원회를 열고 ‘임상재평가 결과보고서 제출기한 연장 사유의 타당성 및 연장 기간의 적정성 자문’ 건을 논의하고 제약사들의 연장 요청을 수용했다. 종근당이 진행 중인 경도인지장애 임상은 15개월, 대웅바이오가 진행중인 알츠하이머 임상은 24개월 연장됐다. 의약품 재평가 실시에 관한 규정에 따르면 제약사들은 1회에 한해 최대 2년까지 기한 연장을 요청할 수 있다.
치매 치료 등에 사용되는 콜린알포는 2021년부터 식약처 조치에 따라 효능을 다시 입증하는 임상 재평가가 진행 중이다. 한국이 약가 정책에 참고하는 8개 국가(A8) 중 원개발국인 이탈리아를 제외한 모든 국가가 해당 의약품을 전문의약품으로 인정하지 않고 급여 역시 반영되지 않고 있기 때문이다.
이번 연장은 전공의 집단 사직에 따라 제약사들이 임상 대상자 모집에 어려움을 겪은 것을 고려한 조치로 알려졌다. 식약처는 올해 한약(생약)제제 의약품들 재평가에서도 전공의 사직이 업체가 예측할 수 없던 천재지변 같은 부득이한 사유에 해당한다고 판단해 기한을 연장했다.
제약사들은 효능 입증에 실패할 경우 계획서를 승인 받은 날부터 삭제일까지 처방액 20%를 건강보험공단에 환급해야한다. 남인순 더불어민주당 의원실에 따르면 지난해 국내 콜린알포 제제 처방액은 5734억원으로 2018년 2739억원 대비 109.4% 늘었다. 종근당과 대웅바이오는 콜린알포 시장의 40%를 차지하는 만큼 환수액이 수천억 원에 달할 수 있다는 전망도 나온다.
< 저작권자 ⓒ 서울경제, 무단 전재 및 재배포 금지 >








 1min9@sedaily.com
1min9@sedaily.com